Хороший, злой кислород: за что присудили Нобелевскую премию по медицине и физиологии в 2019 году
Объясняем простыми словами, в чем польза и значимость «нобелевского» открытия
В этом году Нобелевскую премию по медицине получили два американских и один английский ученый. Они установили, что все клетки в человеческом организме включают сигнал тревоги при нехватке кислорода. И многие раковые опухоли умудряются имитировать эти сигналы, чтобы получить необходимый для роста кислород. Ученые же долгое время не знали о том, как именно работает «тревожная кнопка», а просто наблюдали за процессами. Результатом открытий (сделаны они были еще в 90-е годы) может стать лекарство от анемии и в перспективе — очередная панацея от рака.

Чтобы понять важность «нобелевского» открытия, придется вникнуть в краткую вводную часть о значимости кислорода. Для чего он нужен? «Чтобы дышать», но не только: кислород помогает превратить пищу в полезную энергию. 80% кислорода, который мы вдыхаем, потребляют митохондрии. Митохондрии, как точно и лаконично определяет их учебник биологии, — «энергетические станции» клетки. За счет расщепления глюкозы, полученной из пищи, митохондрии высвобождают энергию, которая поставляется для синтеза белков, углеводов, жиров и так далее.
В ходе эволюции появились механизмы, которые обеспечили ткань и клетки достаточным количеством кислорода. Однако иногда отлаженная система дает сбой. На это ученые стали обращать внимание еще в начале ХХ века. Так, в 1938 году бельгиец Корнел Хейманс получил Нобелевскую премию, установив зависимость частоты дыхания от уровня кислорода в крови. Оказалось, что в сонных артериях есть специальные клетки, которые измеряют уровень кислорода в крови. Если кислорода недостаточно, «спецклетки» посылают тревожные импульсы в мозг. Мозг дает сигнал увеличить вентиляцию легких и повысить артериальное давление, в результате чего улучшается снабжение организма кислородом. Открытие нобелевских лауреатов 2019 года по сути затрагивает ту же проблему — как адаптируется организм к разным уровням кислорода.
Первый неизвестный
То, что клетки чувствуют снижение уровня кислорода и сигнализируют об этом «соседям», ученые знали и прежде. Загадка состояла в том, как именно они это делают? Кто кислородный информант? Ответ на этот вопрос, скорее всего, обогатит словарный запас читателя несколькими новыми понятиями.
Итак, есть почки. И есть гипоксия (нехватка кислорода. — примеч. Daily Storm). Когда организму не хватает кислорода, в почках вырабатывается гормон под названием эритропоэтин (ЕРО). Он в свою очередь отвечает за производство эритроцитов, или красных кровяных клеток. Их задача — доставлять кислород от легких к тканям тела. Грубо говоря, чем меньше в организме кислорода, тем скорее эритропоэтин пытается его восполнить за счет собственной «службы доставки». Эритропоэтин выделяется, например, при занятии спортом или при подъеме в горы. А также при почечной недостаточности, которая вызывает анемию.

В 1990-е годы Грегг Семенца изучал гормон EPO и то, как он реагирует на гипоксию. Питер Рэтклифф также работал над этой темой. Однако в трудах ученых было недостающее звено — непонятно, что именно запускает работу EPO в условиях нехватки кислорода.
В 1993 году поиски увенчались успехом. Семенца обнаружил белковый комплекс, которому дал говорящее название — HIF — hypoxia-inducible factor, то есть фактор, вызванный гипоксией. Затем выяснилось, что HIF напрямую связан с ДНК. Это значит, что все клетки тела восприимчивы к нехватке кислорода, а не только клетки почек, как это считалось раньше. Следовательно, ЕРО под силу спасти все ткани, страдающие кислородным голоданием.
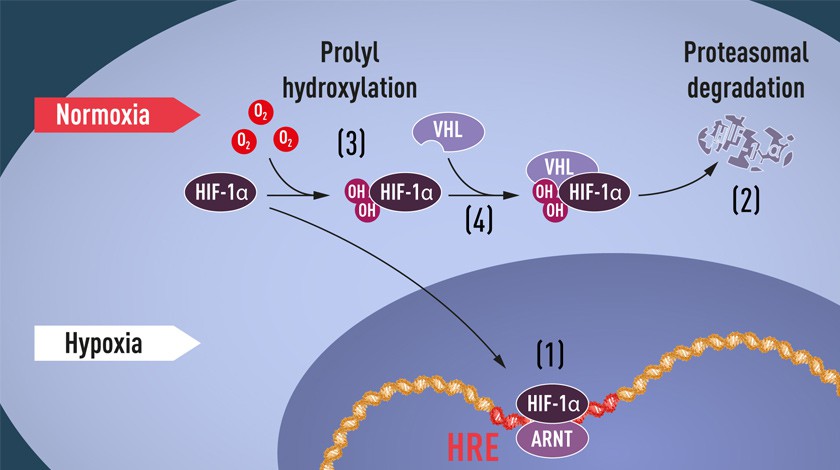
Стало ясно и то, что количество HIF в клетке может меняться. Когда в теле мало кислорода, количество HIF растет. Но когда кислорода достаточно, HIF не активен, вплоть до того, что за своей ненадобностью расщепляется в цитоплазме. Аппарат, который «убивает» нерабочие клетки, называется протеасома (кстати, за его открытие в 2004 году тоже присудили Нобелевскую премию). Однако протеасома не сама принимает решение — кого оставить, а кого расщепить. В этом ей помогает «черная метка». Белки, предназначенные для утилизации, снабжаются специальной меткой в виде небольшого белка убиквитина. В момент насыщения кислородом к HIF пристраивается судьбоносная молекула, и белок маркируется как мусор.
Таким образом, ученые изучили эритропоэтин, выяснили, что HIF активирует производство ЕРО, но до сих пор не установили, как убиквитин связывается с HIF зависимым от кислорода образом.
Второй неизвестный
Тут в игру включился третий лауреат, Уильям Кейлин, и клубок стал потихоньку распутываться.
Примерно в то же время, когда Семенца и Рэтклифф работали над геном ЕРО, исследователь рака Уильям Кейлин изучал наследственный синдром, болезнь Гиппеля — Линдау (болезнь VHL). Она встречается у одного человека из 36 тысяч. Болезнь Гиппеля — Линдау повышает риск развития некоторых форм рака, виной тому — мутация, или «поломка» гена VHL.

Кейлин показал, что клетки, лишенные здорового гена VHL, производят аномально много генов, появляющихся при гипоксии. То есть в отсутствие VHL клетка почему-то пытается восполнить кислород, которого и так хватает. Но когда VHL вновь вводится в клетки, нормальный уровень кислорода восстанавливается. Это дало понять, что VHL является частью комплекса, который маркирует белки убиквитином, иначе говоря, VHL — один из контролеров, который расставляет «черные метки».
Затем Рэтклифф сделал ключевое открытие: при нормальном уровне кислорода VHL взаимодействует с HIF, помечает его убиквитином и «тащит» в цитоплазму, чтобы тот спокойно разлагался. Однако поломанный VHL с этой задачей не справляется, и этим нагло пользуются раковые опухоли. Ведь чтобы расти, раковым клеткам необходим кислород и питательные вещества. Многие опухоли «обманывают» белок HIF, посылают тревожные сигналы, что «задыхаются», и тем самым заставляют HIF работать постоянно. Происходит рост сосудов в окружающей ткани. И наоборот. блокировка HIF тормозит рост раковых клеток. Пазл наконец сложился.
Полезность открытия
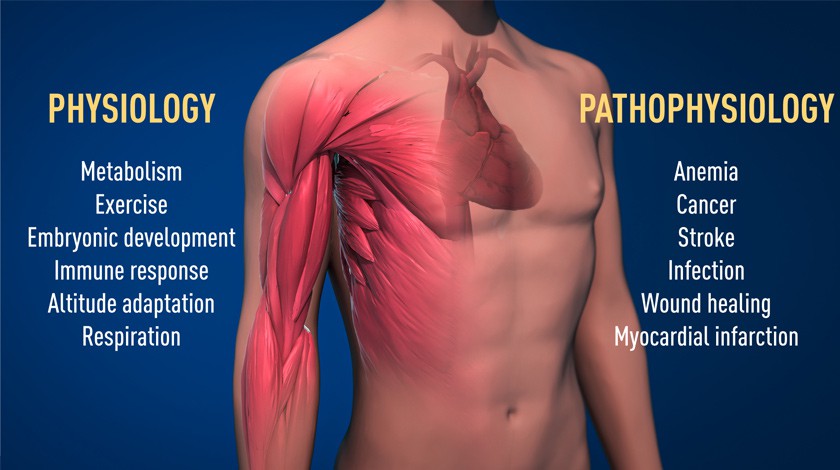
Благодаря нобелевским лауреатам мы узнали гораздо больше о том, как различные уровни кислорода регулируют важные для жизни процессы. Наша иммунная система и многие другие физиологические функции настраиваются с помощью O2. Кроме того, в вопросе снабжения клеток кислород занимает центральное место в анализе большого числа заболеваний. И если в одном случае следует сократить поставку кислорода (как при заболевании раком), то в других необходимо ее увеличить. Например, пациенты с хронической почечной недостаточностью часто страдают от тяжелой анемии из-за снижения выработки ЕРО. В отдельных клиниках уже разрабатываются лекарства, которые могут воздействовать на разные болезни, активируя или блокируя чувствительность к кислороду.

