
Сильный слабый литий: как открытие нобелевских лауреатов заложило основу беспроводной электроники
Просто и доступно — о Нобелевской премии по химии за 2019 год
Если днем ранее премию по физике вручили за исследования, о которых рассказывают даже гуманитариям на первом курсе университета, то премию по химии и вовсе дали за открытие, результатами которого все пользуются последние 30 лет. Речь о литийионном аккумуляторе. Эта легкая, перезаряжаемая и мощная батарея теперь применяется везде: от мобильных телефонов до электромобилей. По сути, мы регулярно носим «Нобелевскую премию» в кармане или сумочке. Кроме того, такая батарея способна накапливать солнечную и ветровую энергии. В будущем это позволит отказаться от ископаемого топлива.

Практически вся портативная электроника сегодня сидит на «литиевой игле». Однако всеобщего признания этот металл ждал довольно долго. Литий — древний элемент, который появился в первые минуты Большого взрыва. Человечество узнало о нем в 1817 году благодаря шведским химикам Иоганну Арфведсону и Йенсу Берцелиусу, которые очистили его из образца минерала. Свое название литий получил из-за того, что был найден в «камне» («литос» с греч.), а точнее — в шахте Стокгольмского архипелага.
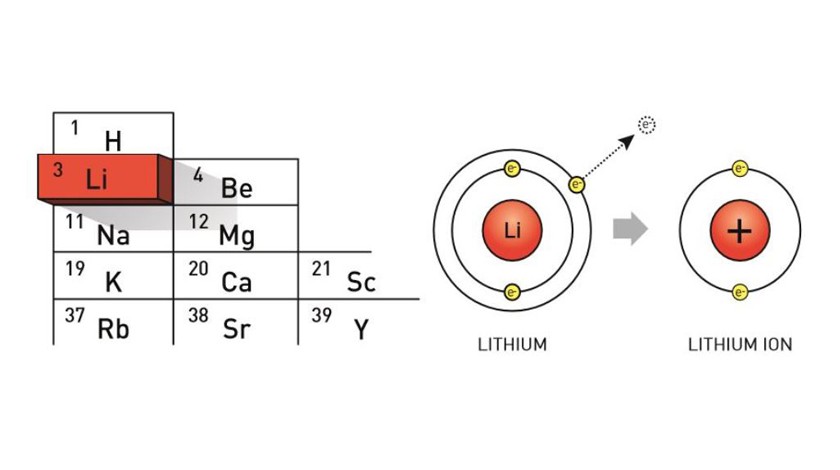
Несмотря на свое тяжеловесное название, литий — легкий элемент, собственно, поэтому мы без труда везде таскаем с собой мобильник. Литий имеет только один электрон на внешней электронной оболочке и при удобном случае стремится поскорее с ним расстаться, то есть вступить в реакцию с другим элементом из таблицы Менделеева. Когда это происходит, вместо лития образуется ион лития, заряд меняется с отрицательного на положительный и вещество становится более стабильным. Последнее особенно важно. Литий в чистом виде крайне опасен, при попадании на влажную кожу и слизистые оболочки он вызывает ожоги. А при контакте с кислородом может воспламениться и взорваться.
Уиттингем и чрезвычайная энергоемкость
Первые шаги на пути к созданию литийионной батареи были сделаны почти полвека назад. Тогда (впрочем, как и сейчас) экологическая повестка сильно вклинивалась в разработки ученых. В 1970-х за окном стоял нефтяной кризис, и энергетические компании всерьез задумывались об ограниченности ресурса, а попутно и о том, что дышать выхлопными газами становится как-то сложно. Нужно было искать альтернативные источники энергии, и желательно такие, которые никогда не иссякнут.
Нефтяной гигант, компания Exxon, приняла вызов и наняла лучших исследователей в этой области. Среди них оказался британец Стенли Уиттингем. Ученый и его коллеги начали изучать сверхпроводящие материалы, в том числе соль с постапокалиптическим названием «дисульфид тантала» (TaS2). Важно отметить, что некоторые соединения могут интеркалировать, то есть включать в себя заряженные ионы других элементов, тем самым наращивая мощность. Дисульфид тантала был как раз такой. Выискивая наиболее мощные связи, ученые интеркалировали соль разными ионами. На удивление взаимодействия между ионами калия и дисульфидом тантала были очень энергоемки, настолько, что можно было рассчитывать на получение пары вольт напряжения. Этот показатель был выше, чем у всех батарей того времени.
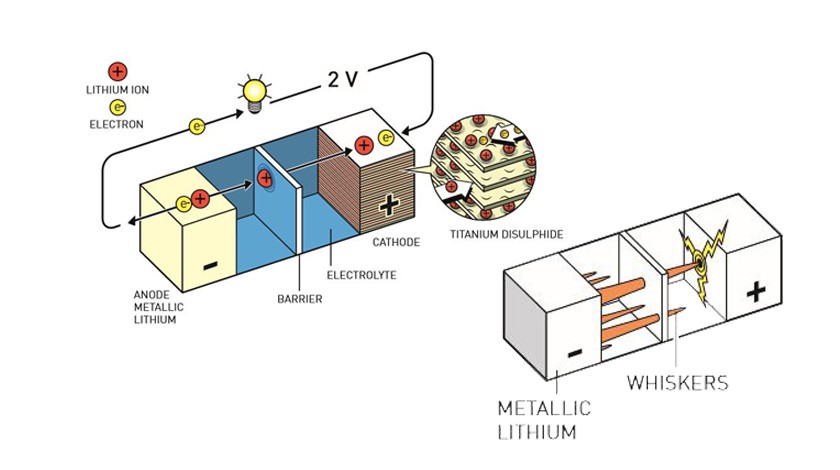
Литий справлялся с задачей еще лучше. Как известно, у любой батарейки есть плюс (катод) и минус (анод). Из анода пучок тока уходит, а в катод — приходит. Ток, то есть движение электронов, образуется за счет некоторых химических реакций. Когда литий отдает титану свой единственный электрон, то возникает тоже своего рода ток. Зная тягу лития к расставанию с электронами, ученые сделали из него анод, а из дисульфида титана (титан в итоге оказался предпочтительнее тантала) — катод. Когда литий терял электрон, то в виде иона включался в дисульфид титана, и батарея работала. А когда батарею ставили на зарядку, то ионы переходили обратно в анод (интеркаляция — обратимый процесс), и литий восстанавливался. Таким образом, пользоваться «химической» батарейкой можно было несколько раз.
Однако возник ряд проблем. Хотелось, чтобы аккумулятор был более долговечным, а для этого нужно найти катодный материал, который бы стойко переживал входы и выходы ионов лития. Иначе катод разрушался.
К тому же металлический литий был все еще реактивен. Батарея оказалась слишком взрывоопасной, и эксперименты пришлось прекратить. К тому же произошел очередной обвал цен на нефть — спонсировать опыты стало невыгодно.
Гуденаф и четыре вольта
Немец Джон Гуденаф, занимавший в это время должность профессора неорганической химии в Оксфорде, знал об инновационной батарее Уиттингема. Однако что-то подсказывало ему: будь на месте дисульфида титана оксид металла, батарея стала бы мощнее. Ученый распорядился найти оксид металла, который бы вырабатывал более высокое напряжение и не разрушался ионами. Поиск увенчался большим успехом, да таким, что сам Гуденаф был поражен.
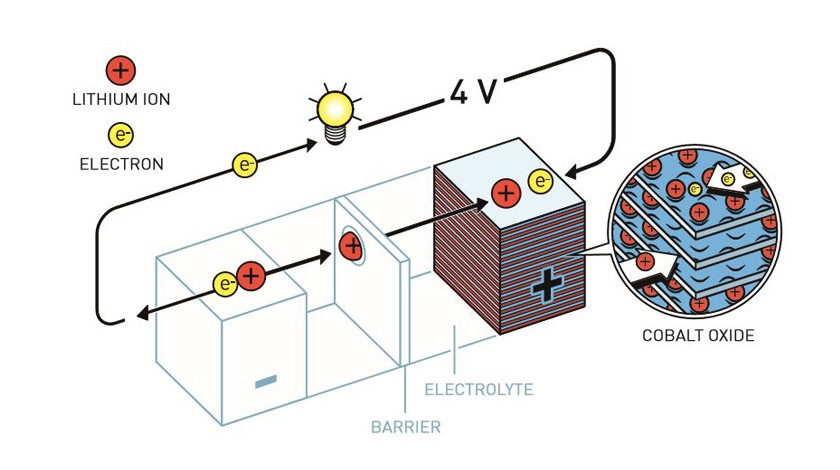
Новым героем этой истории стал оксид кобальта. Поместив его в катод, ученый создал аккумулятор, который генерировал почти четыре вольта напряжения, что в два раза превышало показатели Уиттингема.
В 1980 году Гуденаф опубликовал сведения об открытии этого нового энергоемкого катодного материала, который, несмотря на его небольшой вес, привел к созданию мощных аккумуляторов высокой емкости. Но в то же время проблема с возгоранием лития до сих пор не была решена.
Йошино и та самая литиевая батарейка
Если на Западе интерес к альтернативным источникам энергии временно утих, то в Японии, наоборот, возрос. Компании-производители остро нуждались в легких и перезаряжаемых батареях для питания новой чудо-техники: видеокамер, беспроводных телефонов и компьютеров.
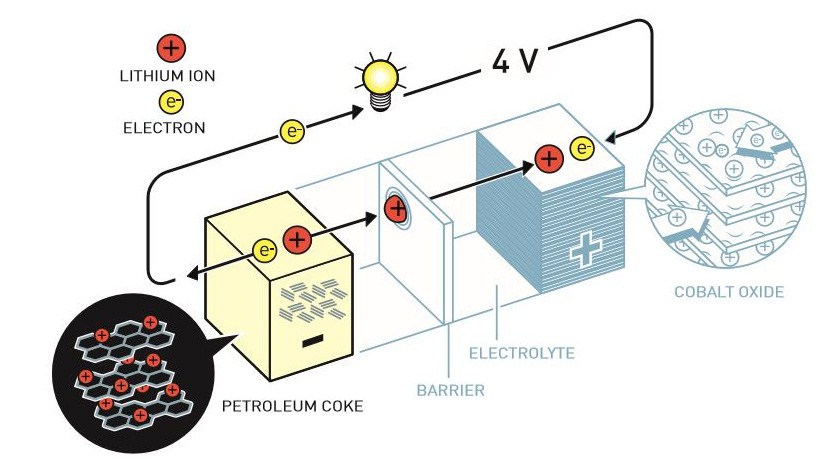
В 1985 году Акира Йошино создал первую жизнестойкую литийионную батарею. Вместо того чтобы использовать реактивный литий в аноде, ученый заменил его на углеродный материал — нефтяной кокс. Он также может включать в себя ионы лития. А в качестве катода химик применил оксид лития-кобальта, то есть соединил в одно два вещества, которые раньше находились на противоположных полюсах аккумулятора, тем самым «припрятав» чистый литий от окружающей среды. Когда Йошино включал, «расходовал» батарейку, то ионы лития примыкали к оксиду кобальта. А когда заряжал батарейку, ионы перетекали обратно в сторону нефтяного кокса, где находили стабильность и спокойствие. Таким образом, ионы путешествовали туда-сюда, не производя никаких химических реакций. Контакта с окружающей средой не было, а значит не было и шансов на возгорание. Батарейка выдавала все те же четыре вольта и больше не взрывалась.
Таким образом, Уиттингем создал энергоемкий носитель, Гуденаф добавил ему мощности, а Йошино сделал безопасным. В результате получился легкий износостойкий аккумулятор, который можно заряжать сотни раз, прежде чем он придет в негодность. Литийионные батареи произвели революцию в нашей жизни, когда впервые появились на рынке в 1991 году. Они заложили основу беспроводной электроники и снизили зависимость общества от исчерпаемых ресурсов.

